زئولیتها آلومينوسيليكات هاي آبدار و بلورين با فلزات قليايي و قليايي خاكي مثل سدیم، پتاسیم، کلسیم و منیزیوم هستند. این کانی ها از نظر ساختاری، مواد معدنی بلوری پیچیدهای هستند که از چهار وجهی متصل به هم و نامحدود SiO4 و AlO4 تشکیل شده اند و هر اکسیژن بین دو چهاروجهی در اشتراک است. سيليسيوم یک کاتیون ۴ بار مثبت (Si4+) و آلومينيم یک کاتیون ۳ بار مثبت (Al+3 ) است. در زمان تشکیل این کانی Al+3 جایگزین Si4+ میشود و بنابراین به ازاي هر چهار وجهي AlO4 یک سیلیسیوم از شبکه خارج شده و يك بار منفي ايجاد ميشود. این بارهای منفی حاصل از جانشینی هم شکل Al به جای Si، توسط كاتيونهاي قرار گرفته در شبكه خنثي ميشوند.
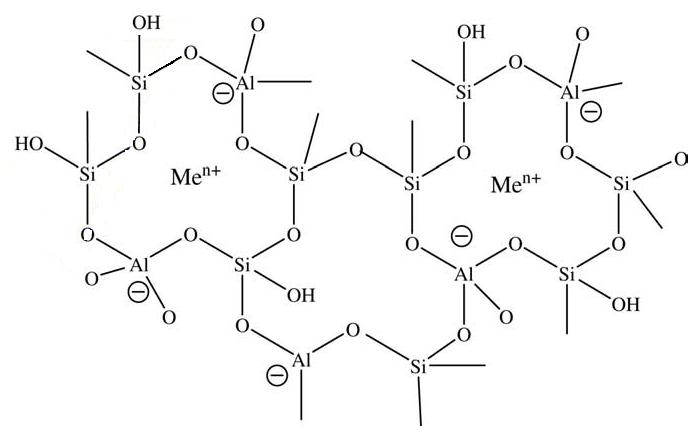
فرمول تجربی ارائه شده برای زئولیت به صورت M2/nO.Al2O3.xSiO2.yH2O میباشد. در این فرمول M نشان دهنده يك يا چند كاتيون با ظرفیت n است و ميتواند هر يك از فلزات سديم، پتاسيم، منيزيم يا كلسيم باشد. x عددي است كه بسته به نوع زئوليت بين ۲ تا ۱۰ تغيير میكند و به نحوی به جایگزینی هم شکل آلومینیوم به جای سیلیسیم اشاره می کند. y تعداد مولكول هاي آبی که در ساختار زئولیت وجود دارد را نشان ميدهد ( شکل ۱)..

شکل ۱- ساختمان ملکولی زئولیت
کانی زئولیت از تجمع واحدهای سازنده زئولیت که آن هم از کنار هم قرار گرفتن چهار وجهي هاي آلومینیوم و سیلسیوم به وجود آمده اند، تشکیل میشود. یعنی چهاروجهی های اولیه در قالب های مكعبی، منشور شش ضلعي و يا مكعب هشت وجهي کنار هم قرار گرفته و واحدهاي سازنده ثانويه را تشکیل میدهند. این واحدهای ثانویه به صورتهای متنوعی در سلسله مراتب مختلف با هم ترکیب میشوند و ساختار زئولیت را میسازند. در شکل ۲ واحدهای سازنده و ساختمان زئولیت آورده شده است.


شکل ۲- واحد های سازنده و ساختار زئولیت
شبکه تشکیل یافته زئولیت در سه بعد به صورت نامحدودی گسترش مییابد و در فضای بین آن كانال ها و حفرات متصل به هم ایجاد میگردد که بوسيله كاتيون ها و مولكول هاي آب اشغال میشود. کاتیونهای موجود در این ساختار متحرک هستند و میتوانند با سایر کاتیون ها جایگزین شوند. این ویژگی ظرفیت تبادل كاتيوني را براي زئوليت به وجود ميآورد. ملکول های آب نیر می توانند به صورت برگشت پذیر و پیوسته از شبکه خارج شوند و یا وارد آن شوند. دمای لازم برای خروج کامل آب از ساختار زئولیت و دهیدراته شدن آن حدود ۴۰۰ درجه سانتیگراد می باشد. به دلیل همین مشخصات است که زئولیت قابلیت جذب آب، بخارات، کاتیونهای مختلف، فلزات سنگین، گازها و به ويژه مولكول هاي قطبي را دارد.
کلینوپتیولایت (Clinoptilolite) کانی زئولیت طبیعی است که به وفور یافت می شود و در معادن ایران نیز شناسایی شده است. این کانی در سنگهای رسوبی که منشا آتشفشانی دارند، وجود داشته و از درجه خلوص بالایی برخوردار است. فرمول تجربی زئولیت کلینوپتیولایت به صورت (Na,K,Ca)6(Si30Al6O72) •۲۰H2O برای واحد ساختمانی میباشد. ظرفیت تبادل کاتیونی این نوع زئولیت حدود ۲۰۰ تا ۲۶۰ میلی اکیوالان بر صد گرم است و از این نظر می تواند در بسیاری از واکنشهای خاک نقش فعالی داشته باشد. شرکت ژرف کام پایدار مفختر است که ضمن معرفی زئولیت معدنی، آن را به صورت تخصصی در اختیار مصرف کنندگان قرار میهد.
